
Розвиток сучасної науки та її прикладних напрямів відбувається в усіх галузях людської діяльності. Нові технології все частіше знаходять застосування навіть в одній із наконсервативніших галузей сільського господарства – тваринництві. Впровадження наукових технологічних розробок дає відчутні результати на таких етапах як годування тварин, кормовиробництво, утримання поголів’я, швидкісне вирощування м’ясного молодняка тощо. Крім того, більш вагомого значення набуває генна інженерія. Вміння штучно змінювати набір генів тварин відкриває величезні перспективи перед вченими, тваринниками та людством загалом.
Коли заходить мова про трансгенних тварин, більшість з нас створює у своїй уяві якийсь фантастичний образ страшої істоти-конструктора, в якій поєднані частини тіл різних тварин. А вчених, що займаються трансгенною роботою, багато хто сприймає як злих геніїв, які ведуть цивілізацію до неминучої загибелі. Проте на практиці все виглядає зовсім інакше. І хоча деякі трансгенні тварини, створені заради експерименту (наприклад, миші, що світяться в темряві) зовні відрізняються від звичайних, здебільшого вони зберігають свій природний вигляд.
Головними критеріями у створенні трансгенних особин є їх якісні та кількісні показники продуктивності, а не зовнішні ознаки. Генномодифіковані тварини створюються переважно не задля розваги, а для раціонального вирішення глобальних проблем, пов’язаних з подальшим існуванням людства.
Основні цілі втручання в генетичну суть живих організмів полягають у зміні властивостей тварин в потрібному для людини напрямі, набутті ними нових можливостей, а також усуненні деяких негативних якостей. За допомогою генної інженерії вчені створюють тварин з особливими, незвичайними параметрами продукції, тварин, стійких до різних хвороб, тварин з підвищеною продуктивністю тощо.
Так, наприклад, створені й успішно використовуються вівці, цілком звичайні на вигляд, які виробляють молоко, що містить фермент хімозин або сичужний фермент. У молокопереробній галузі він має неабияке значення для виробництва твердих сортів сиру. Раніше його отримували тільки з ґляґу (сичугу) – частини багатокамерного шлунку новонароджених жуйних тварин: телят, ягнят, козенят. Задля цього молодняк забивали в перші ж дні його життя.
Зараз одна трансгенна вівця за лактаційний період (кілька місяців) виробляє таку кількість хімозину, якого вистачає для виробництва тридцяти тонн твердого сиру! Поголів’я генномодифікованих, «хімозинових» овець налічує сьогодні цілу отару! І можна лиш уявити, скільки новонародженого молодняка жуйних тварин збереглось завдяки цьому досягненню генної інженерії.

Якщо продовжити тему сиру та трансгенних тварин, то в Англії існує велике стадо генномодифікованих корів, які продукують молоко з ідеальним складом для виробництва сиру «Чеддер», який так цінується в усьому світі. А ще створили корів, у молоці яких вміст речовин, здатних викликати алергічні реакції, значно знижений. Водночас кількість у ньому кальцію та деяких вітамінів – збільшена.

Вже отримані трансгенні риби декількох видів, до генетичного коду яких додано ген, який кодує підвищений синтез соматотрофного гормону (гормону росту), завдяки чому риба росте швидше, до того ж значно перевершує свої звичайні розміри. Прикладом є атлантичний лосось фірми «AquaBounty», котрий розвивається вдвічі швидше звичайного.
Щоб досягти такого ефекту, звичайному лососю вживили ділянку гена вугреподібної риби бельдюги американської, який підвищує продукування соматотрофного гормону в організмі лосося, причому незалежно від температури води. М’ясо нового лосося нічим не відрізняється від м’яса інших представників цього виду, але час вирощування товарної риби скорочується вдвічі!
Результати, досягнуті в іншому прикладі перенесення генів, є ще більш вражаючими. Внаслідок введення в ядра запліднених ікринок риби нерка генетичної інформації, що кодує посилене продукування гормону росту, однорічні трансгенні нерки, які з’явилися з цих ікринок, важили в середньому в 10 разів більше, ніж їхні нетрансгенні ровесники!

За допомогою генної інженерії також створені свині, яким доданий геном, що кодує продукування травного ферменту фітази. Такі тварини краще перетравлюють і засвоюють корм, завдяки чому підвищується його конверсія та прискорюється ріст свиней. Я наслідок, при тих самих витратах корму істотно підвищується продуктивність тварин, і тваринники отримують від таких свиней значно більше м’яса.
Створення сільськогосподарських тварин, стійких до основних захворювань, які завдають відчутного матеріального збитку господарству і навіть можуть передаватися людині, має великі економічні перспективи, тому що це допоможе уникнути витрат на профілактику, лікування, усунення наслідків захворювань (дезінфекція, утилізація загиблих тварин, карантинні обмеження тощо), а також недоотримання продукції.
Наприклад, проводяться дослідження з вирішення проблеми лейкозу великої рогатої худоби, який спричинюють РНК-віруси. Введення в ядро генів, що кодують антисенсові РНК, теоретично має зробити ВРХ стійкою до лейкозу. Експерименти на кролях вже продемонстрували позитивний результат. Ще одне з подібних досягнень – свині, поросята яких резистентні до діареї, що значно полегшує їх вирощування.
Вже зараз існують корови з генами зебу, яким властива нечутливість до багатьох кровопаразитарних захворювань. Додані в геном великої рогатої худоби гени зебу кодують одразу кілька ознак, завдяки чому отримані трансгенні тварини окрім стійкісті до хвороб набули водночас підвищеної жаровитривалості та невибагливості до кормової бази.

Але генні модифікації можна застосовувати не лише для вирішення продовольчих і економічних завдань. Завдяки використанню генної інженерії можна задовольняти багато людських потреб у педіатрії та медицині в цілому. Наприклад, одна з груп генномодифікованих корів здатна давати молоко, що містить людський білок лактотрансферин (у молоці звичайних корів цієї речовини немає). Лактотрансферин є важливою складовою гуморального імунітету, він має противірусну, антибактеріальну, протигрибкову, антипаразитарну дію, а також каталітичну активність і використовується при штучному вирощуванні новонароджених дітей.
Також ведеться робота зі створення свиней, здатних продукувати людський інтерферон, якого дуже потребує фармацевтична галузь. Від модифікованих тварин (корів, свиней, кіз, кроликів, овець) вже вдалося отримати вісімнадцять лікарських білків. Такі живі біологічні фабрики значно рентабельніші, ніж аналогічне за продуктивністю промислове виробництво необхідних речовин.
У Великобританії вчені-генетики створили трансгенних курей, яйця яких містять лікувальний білок з miR24-молекулою та людський інтерферон b-1a. В обробленому вигляді ці речовини використовуються як сировина у виробництві препаратів, призначених для лікування артритів, множинного розсіяного склерозу та злоякісних пухлин у людини.
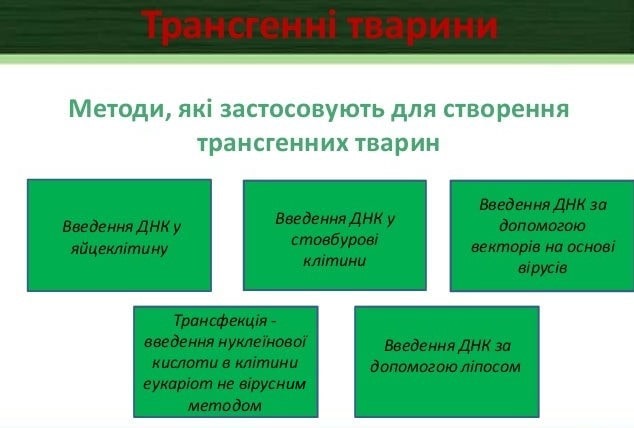
Але як створюють трансгенних тварин? Цей процес дуже тривалий і непростий. Існує кілька основних методів створення генних модифікацій у вищих тварин:
– пронуклеарна мікроін’єкція;
– використання вірусних конструкцій;
– використання ембріональних стовбурових клітин.
З них найбільш зручний та найчастіше використовуваний – це метод пронуклеарної мікроін’єкції. Переваги його полягають у тому, що він є універсальним: з його допомогою можна втручатися в геном будь-яких тварин. Цей метод дозволяє отримати швидкий результат: необхідні показники проявляються вже в першому поколінні. Він не має обмежень щодо розміру впроваджуваної ділянки ДНК. Якщо під час використання вірусних конструкцій можна вставити лише 8–10 тисяч пар нуклеотидів, то за допомогою пронуклеарної мікроін’єкції можна ввести у кілька разів більше – 100 тисяч і навіть кілька мільйонів пар нуклеотидів! Тобто, достатньо одного втручання, щоб ввести набагато більше цільової генетичної інформації.
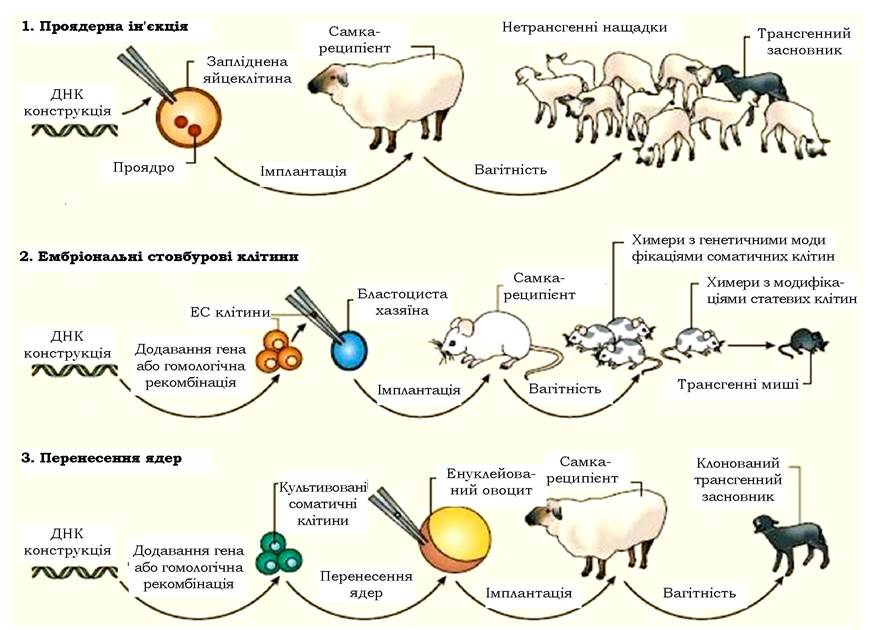
Суть цього способу полягає в наступному: у відібраних самок тварин запліднюють яйцеклітини, що вийшли внаслідок штучно стимульованої овуляції. Потім, або в ядро чоловічого пронуклеуса, або в ядро клітини, що утворилася, на стадії зиготи за допомогою спеціального обладнання (мікроманіпулятора) впроваджують потрібну ділянку ДНК (або генну конструкцію). Зиготу впродовж тижня після впровадження (за цей час цільовий ген вбудовується в геном клітини-рецепієнта і змінена клітина починає розвиватись у багатоклітинний модифікований організм) культивують у живильному середовищі з високим вмістом вуглекислого газу (5%, як і в живих тканинах організму ссавців), після чого на стадії морули або ранньої бластоцисти пересаджують у матку сурогатної матері.
Великим тваринам – коровам, кобилам, верблюдицям – пересаджують по дві зиготи, козам та вівцям по 3–4, свиням і кролихам по 20–30. Приплід після народження перевіряють на присутність потрібної генетичної інформації та, у разі позитивного результату, розводять «в собі» як основу майбутньої трансгенної популяції, застосовуючи відбор та підбір, традиційні для звичайної племінної роботи. Молодняк, народжений від трансгенних тварин, успадковуює його модифікований набір генетичної інформації та пов’язані з ним властивості в усіх наступних поколіннях.
Вже достатньо добре відпрацьовані технології генних модифікацій для таких видів риб як форель, короп, лососеві. Вони полягають у тому, що необхідні ділянки ДНК вводять до запліднених ікринок за допомогою мікроін’єкції. Розвиток модифікованої ікри протікає у воді, у ванних кімнатах з регульованими параметрами мікроклімату. Після ін’єкцій чужорідних генів виживає приблизно від 35 до 80% ембріонів. З них успішно приймають нові гени у свій генетичний набір від 10 до 70%. Тобто, у промислових риб ефективність перенесення потрібної спадкової інформації порівняно висока. Проводиться робота з впровадження генів, які збільшать стійкість риби до хвороб та несприятливих впливів навколишнього середовища.
Далеко не всі спроби генних маніпуляцій завершуються успіхом. На кожному етапі кількість ембріонів постійно зменшується на 10–20% з різних причин. Якісь гинуть, інших відбраковують самі вчені. З тисячі яйцеклітин можна отримати лише кілька вдалих трансгенних тварин. Технологія мікроін’єкції дає хороші за якістю результати, але дуже дорога. Створення однієї мінімальної популяції з кількох трансгенних тварин коштує від 60 до 300 тисяч доларів США. До того ж, щоб здійснювати необхідні маніпуляції, потрібен мікроманіпулятор та інше вартісне обладнання. Набагато дешевше створювати трансгенних тварин за допомогою вірусів.
Для здійснення цього способу вченим спочатку потрібно створити зі звичайного вірусу псевдовірус. Суть перетворення полягає в тому, що з вірусу видаляють більшість його генів і залишають тільки найнеобхідніші для його виживання, після чого прикріплюють потрібну для створення трансгенної тварини ділянку ДНК. Цим зміненим, відносно нешкідливим вірусом обробляють зиготу.
Вірус проникає в зиготу, самостійно вбудовується в геном зиготи та одночасно вбудовує потрібний ген. Потім зиготу деякий час культивують в інкубаторі і трансплантують у матку сурогатної матері. Коли строк вагітності завершиться, отримують трансгенний молодняк. Це потомство тестують на наявність того гена, який планувалося ввести в його геном, відбирають необхідних особин і розмножують їх із застосуванням жорсткого вибракування тварин, що не відповідають заданим параметрам, штучного відбору та підбору пар, як і в попередньому випадку.
Ефективність такого методу набагато вища, ніж мікроін’єкції – вона становить до 70%! Але в нього є й недоліки: не лише чужий ген діє на геном ембріона, а й сам геном чинить вплив на чужорідний ген, змінюючи його роботу. Якщо вірус вбудувався в ділянку ДНК ембріона, яка активно не працює, то і цей цільовий ген теж не працюватиме, незважаючи на свою присутність у геномі трансгенної тварини. Вперше віруси для перенесення гена використав німецький біолог Рудольф Яніш у 1970 році.
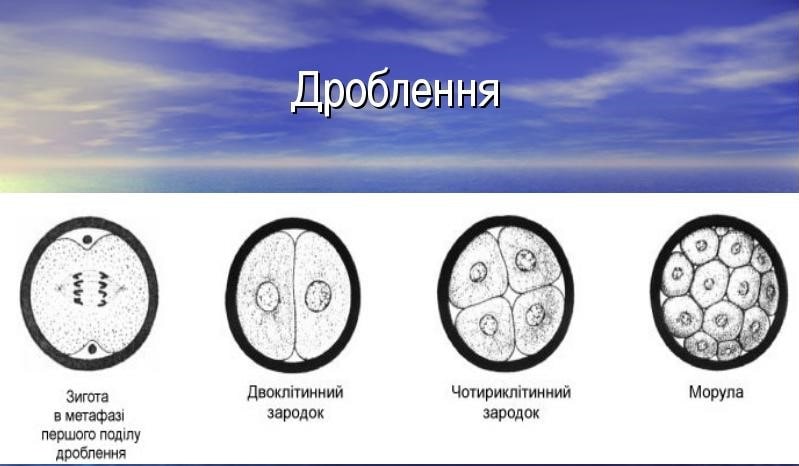
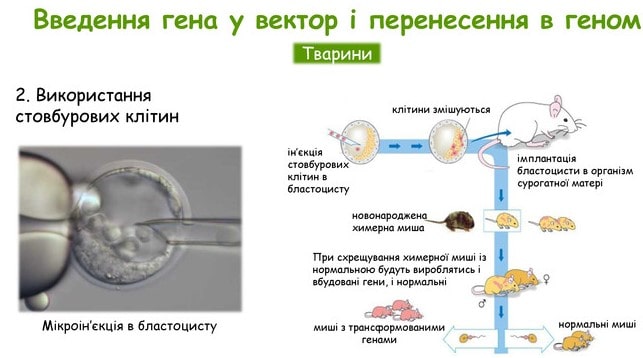
Метод створення трансгенних організмів із застосуванням ембріональних стовбурових клітин практикуют здебільшого в наукових дослідженнях, а не для модифікації продуктивних сільськогосподарських тварин. Цей процес у спрощеному варіанті виглядає таким чином: спочатку з клітинної маси бластоцисти миші отримують ембріональні стовбурові клітини. Потім їх генетично модифікують, вносячи потрібний ген, після чого культивують у живильному середовищі з 5%-вим вмістом вуглекислого газу і вводять у попередньо отримані зиготи на стадії бластоцисти. «Відкориговані» зиготи поміщають у матки сурогатних матерів. Отримане потомство вчені перевіряють на присутність цільового гена, і відібраних трансгенних тварин спарюють між собою, створюючи таким чином цілу трансгенну популяцію для наукових досліджень.
Питання, що виникли під час ознайомлення з цією темою, можна вирішити на нашому форумі.
Віталій Чугуєвець
Поділитись в соцмережах:







